BIENVENIDOS AL BLOG DE REFUERZO
REALIZAR RESUMEN DE CADA TEMÁTICA
PRESENTAR BLOG DEL 16 AL 21 DE MAYO
REALIZAR LAS ACTIVIDADES
AROMATICOS . Estructura
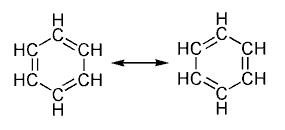
Una característica de los hidrocarburos aromáticos como el benceno, anteriormente mencionada, es la coplanaridad del anillo o la también llamadaresonancia, debida a la estructura electrónica de la molécula. Al dibujar el anillo del benceno se le ponen tres enlaces dobles y tres enlaces simples. Dentro del anillo no existen en realidad dobles enlaces conjugados resonantes, sino que la molécula es una mezcla simultánea de todas las estructuras, que contribuyen por igual a la estructura electrónica. En el benceno, por ejemplo, la distancia interatómica C-C está entre la de un enlace σ (sigma) simple y la de uno π(pi) (doble).
Todos los derivados del benceno, siempre que se mantenga intacto el anillo, se consideran aromáticos. La aromaticidad puede incluso extenderse a sistemas policíclicos, como el naftaleno, antraceno, fenantreno y otros más complejos, incluso ciertos cationes y aniones, como el pentadienilo, que poseen el número adecuado de electrones π y que además son capaces de crear formas resonantes.
Estructuralmente, dentro del anillo los átomos de carbono están unidos por un enlace sp2 entre ellos y con los de hidrógeno, quedando un orbital π perpendicular al plano del anillo y que forma con el resto de orbitales de los otros átomos un orbital π por encima y por debajo del anillo.
[editar]Reacciones
Químicamente, los hidrocarburos aromáticos son compuestos por regla general bastante inertes a la sustitución electrófila y a lahidrogenación, reacciones que deben llevarse a cabo con ayuda de catalizadores. Esta estabilidad es debida a la presencia de orbitales degenerados (comparando estas moléculas con sus análogos alifáticos) que conllevan una disminución general de la energía total de la molécula.
- Sustitución electrofílica (la letra griega Φ se usa para designar el anillo fenil):
- Φ-H + HNO3 → Φ-NO2 + H2O
- Φ-H + H2SO4 → Φ-SO3H + H2O
- Φ-H + Br2 + Fe → Φ-Br + HBr + Fe
- Reacción Friedel-Crafts, otro tipo de sustitución electrofílica:
- Φ-H + RCl + AlCl3 → Φ-R + HCl + AlCl3
Otras reacciones de compuestos aromáticos incluyen sustituciones de grupos fenilos.
Nomenclatura
[editar]Monosustituidos
1.Se conoce muchos derivados de sustitución del benceno cuando se trata del compuesto monosustituidos, las posiciones en el anillo bencénico son equivalentes, los sustituyentes pueden ser alquenilos, alquilos , arilos.2.Nombrar el sustituyente antes de la palabra bencenoNota: Algunos compuestos tienen nombres tradicionales aceptados
Disustituidos
Cuando hay dos sustituyentes en el anillo bencénico sus posiciones relativas se indican mediante números o prefijos, los prefijos utilizados son ORTO, META y PARA, de acuerdo a la forma:•ORTO (o-): Se utilizan en carbonos adyacentes. Posiciones 1,2.•META (m-): Se utiliza cuando la posición de los carbonos son alternados. Posiciones 1,3.•PARA (p-): Se utiliza cuando la posición de los sustituyentes están en carbonos opuestos. Posiciones 1,4.Polisustituidos
•Si hay más de dos grupos en el anillo benceno sus posiciones se deben indicar mediante el uso de números, la numeración del anillo debe ser de modo que los sustituyentes tengan el menor número de posición; cuando hay varios sustituyentes se nombran en orden alfabético.•Cuando algunos de los sustituyentes genera un nuevo nombre con el anillo, se considera a dicho sustituyente en la posición uno y se nombra con el básico..
Benceno como radical
•Pero cuando esta unido a una cadena principal es fenil
Aromáticos Policíclicos
•Para nombrar a este tipo de compuestos se indica el número de posición de los sustituyentes, seguido del nombre del sustituyente y seguido del nombre del compuesto•El orden de numeración de estos compuestos es estricta, no se puede alterar y por ende tienen nombres específicos
Introducción. El bencenoCon este nombre se conocen todos los compuestos derivados del benceno, cuya estructura se muestra a continuación:BENCENO El benceno (C6H6) es un compuesto cíclico de forma hexagonal, compuesto por 6 átomos de carbono y 6 de hidrógeno y tres dobles enlaces alternados. Cada vértice del hexágono, representa un átomo de carbono, al cual está unido un hidrógeno para así completar los cuatro enlaces del carbono.
El benceno (C6H6) es un compuesto cíclico de forma hexagonal, compuesto por 6 átomos de carbono y 6 de hidrógeno y tres dobles enlaces alternados. Cada vértice del hexágono, representa un átomo de carbono, al cual está unido un hidrógeno para así completar los cuatro enlaces del carbono.
El benceno es un líquido volátil, incoloro, inflamable, insoluble en agua y menos denso que ella. Se disuelve en disolventes orgánicos como alcohol, acetona y éter entro otros. Es de olor fuerte pero no desagradable, hierve a 80.1°C y se funde a 5.4 °C. Se obtiene mediante la destilación fraccionada del alquitrán de hulla y es utilizado como solvente de resinas, grasas y aceites; es tóxico y resulta peligroso respirar sus vapores por periodos largos.
Los derivados del benceno se forman cuando uno o más de los hidrógenos son reemplazados por otro átomo o grupo de átomos. Muchos compuestos aromáticos son mejor conocidos por su nombre común que por el sistémico. A continuación se muestran algunos de los derivados monosustituídos más comunes junto con sus características más importantes. El nombre con mayúsculas es su nombre común. El nombre sistémico se presenta entre paréntesis. Las reglas de estos nombres se explicarán más adelante.

Se emplea en la fabricación de explosivos y colorantes. 
Este compuesto no tiene nombre común. Es un líquido incoloro de olor agradable empleado en la fabricación del fenol y del DDT. 
Fue el primer desinfectante utilizado, pero por su toxicidad ha sido reemplazado por otros menos perjudiciales.Se emplea para preparar medicamentos, perfumes, fibras textiles artificiales, en la fabricación de colorantes. En aerosol, se utiliza para tratar irritaciones de la garganta. En concentraciones altas es venenoso. 
Es la amina aromática más importante. Es materia prima para la elaboración de colorantes que se utilizan en la industria textil. Es un compuesto tóxico. 
Se emplea como materia prima de sustancias tales como colorantes. Se utiliza en la fabricación de trinitrotolueno (TNT) un explosivo muy potente. 
Se utiliza como desinfectante y como conservador de alimentos.
Algunos derivados aromáticos están formados por 2 o 3 anillos y les conocen como policíclicos.. Ejemplos:

Es conocido vulgarmente como nafltalina. Es utilizado en germicidas y parasiticidas, además de combatir la polilla. 
Se utiliza para proteger postes y durmientes de ferrocarril de agentes climatológicos y del ataque de insectos. 
Agente cancerígeno presente en el humo del tabaco.
La terminación sistémica de los compuestos aromáticos es benceno, palabra que se une al último sustituyente.En los compuestos disustituídos, dos átomos de hidrógeno han sido reemplazados por radicales alquilo, átomos de halógenos o algún otro grupo funcional como –OH (hidroxi), –NH2 (amino) o –NO2 (nitro) que son los que se utilizarán en los ejemplos.Los sustituyentes pueden acomodarse en 3 posiciones diferentes. Para explicarlas utilizaremos un anillo aromático numerado en el siguiente orden: Las tres posiciones son:
Las tres posiciones son:



Los sustituyentes están en dos carbonos seguidos. Hay un carbono sin sustituyente, entre los que tienen un sustituyente. Los sustituyentes están en posiciones encontradas,. Posiciones Posiciones Posiciones 1,2 2,3 3,4 4,5 5,6 6,1 1,3 2,5 3,5 5,1 1,4 2,5 3,6
Ejemplos:

La posición es meta porque hay un carbono sin sustituyente entre ellos. Esta posición se indica con la letra “m” minúscula y los sustituyentes se acomodan en orden alfabético uniendo la final la palabra benceno y se escribe como una sola palabra Observe que se pone un guión entre la letra de la posición y el nombre del compuesto. m-CLOROMETILBENCENO

Los sustituyentes están encontrados, por lo tanto la posición es para. Se pone la “p” minúscula, y acomodando los radicales en orden alfabético y al final la palabra benceno. p-HIDROXIISOPROPILBENCENO

Los sustituyentes se encuentran en carbonos contiguos, por lo tanto la posición es orto “o”. Se acomodan los sustituyentes en orden alfabético y al final la palabra benceno. o-AMINOISOBUTILBENCENO
Ejemplos de nombre a fórmula:
m-etilnitrobenceno Primero ponemos el anillo y elegimos cualquiera de la posiciones meta y los sustituyentes se pueden colocar indistintamente. 
p-aminoyodobenceno Ponemos el anillo con sustituyentes en posición para, encontrados y colocamos el yodo y el grupo amino indistintamente. 
o-sec-butilhidroxibenceno Se colocan dos sustituyentes en carbonos contiguos en un anillo aromático y se colocan el yodo y el grupo hidroxi en forma indistinta. 
Escriba el nombre o la fórmula según corresponda para los siguientes compuestos.
a) 
b) 
c) 
d) 
e) 
f) 
g) m-cloroyodobenceno h) o-isobutilisopropilbenceno i) phidroxinitrobenceno j) m-aminosec-butilbenceno
Con este nombre se conocen los derivados aromáticos en los cual se han remplazado 3 o más hidrógenos por otros grupo o átomos.De fórmula a nombreEn estos casos es necesario numerar el anillo bajo las siguiente reglas.- El número 1 corresponde al radical con menor orden alfabético.
- La numeración debe continuarse hacia donde este el radical más cercano para obtener la serie de números más pequeña posible. Si hay dos radicales a la misma distancia, se selecciona el de menor orden alfabético; si son iguales se toma el siguiente radical más cercano.
- Todos los átomos de carbono deben numerarse, no solo los que tengan sustituyente.
- Al escribir el nombre se ponen los radicales en orden alfabético terminando con la palabra benceno.
- Como en los compuestos alifáticos, utilizamos comas para separar números y guiones para separar números y palabras.
Ejemplos:

El número 1 corresponde al bromo que es el radical de menor orden alfabético. Se numera hacia la derecha porque en ese sentido quedan los números más pequeños posibles . 1-bromo-3-etil-4-metilbenceno

El radical de menor orden alfabético es el hidroxi, pero a la misma distancia haya dos radicales, por tanto elegimos el nitro que es el de menor orden alfabético y continuamos la numeración en ese sentido. 1-hidroxi-2-nitro-6-n-propilbenceno 
El radical de menor orden alfabético es el sec-butil (recuerde que se alfabetiza por la “b”). Iniciamos ahí la numeración y la continuamos hacia el cloro que es el radical más cercano. 1-sec-butil-2-cloro-4-nitrobenceno

El número 1 coresponde al radical de menor orden alfabético, que es el n-butil. La numeración se continúa hacia la derecha porque el sec-butil tiene menor orden que el ter-butil y ambos están a la misma distancia del número 1. 1-n-butil-2-sec-butil-6-ter-butilbenceno

El número 1 corresponde al amino que es el de menor orden alfabético. A la misma distancia hay un radical isopropil y un radical nitro. Numeramos hacia el isopropil porque tiene menor orden alfabético que el radical nitro. Nombramos en orden alfabético separando las palabras de los números con un guión. 1-amino-4-hidroxi-3-isopropil-
5-nitrobenceno
1,4-dimetil-2-n-propilbenceno
Dibujamos el anillo y lo numeramos. El número 1 se puede colocar en cualquier posición, y por acuerdo numeramos en el sentido de las manecillas del reloj. Podría numerarse en sentido contrario, por eso establecemos que es por acuerdo, no es una regla. Colocamos los radicales en las posiciones indicadas por los números.
1-amino-3-hidroxi-4-nitrobenceno 
No olvide que el anillo hexagonal del benceno tiene 3 dobles enlaces alternados. Iniciamos la numeración en el carbono de nuestra elección, hacia la derecha y colocamos los radicales.
1-sec-buti-5-ter-butil-2-clorobenceno 1-etil-3-isopropil-4-yodobenceno 

1-etil-3-isopropil-4-yodobenceno 1-amino-2-bromo-6-isobutil-3-nitrobenceno 

Escriba el nombre o la estructura según corresponda en los siguientes compuestos.
a) 
b) 
c) 
d) 
e) 
f) 
g) 1-cloro-3-etil-5-isopropilbenceno
h) 1-amino-2-hidroxi-4-metilbenceno
i) m-nitro-n-propilbenceno
j) 1-sec-butil-3-terbutil-5-yodobenceno
k) p-n-butilclorobenceno
I.- Escriba la estructura correcta para los siguientes nombres.1) 1-nitro-3-n-propil-2-yodobenceno2) 1-ter-butil-4-cloro-2-etilbenceno3) o-sec-butilisobutilbenceno4) 1-amino-2-hidroxi-6-isobutilbenceno5) m-bromoisopropilbencenoII. Escriba el nombre que corresponda a los siguientes compuestos. Señale claramente la numeración del anillo.
a) 
b) 
c) 
d) 
e) 
f) 
Cuando el benceno aparece en una cadena como radical se forma un grupo arilo conocido como FENILO. El grupo arilo es un radical cíclico como es el caso del benceno.El anillo aromático se considera radical cuando hay en la cadena principal más de 6 carbonos u otros grupos funcionales.Ejemplo: El carbono unido al radical fenil debe formar parte de la cadena principal. Cuando está junto con otro radical a la misma distancia de los extremos, como siempre, se toma en cuenta el orden alfabético de los radicales.. Ejemplos::
El carbono unido al radical fenil debe formar parte de la cadena principal. Cuando está junto con otro radical a la misma distancia de los extremos, como siempre, se toma en cuenta el orden alfabético de los radicales.. Ejemplos:: En esta estructura hay dos radicales a la misma distancia del extremo pero el de menor orden alfabético es el fenil. Como es un radical todos los grupos funcionales como halógenos y también los enlaces múltiples son más importantes que él.
En esta estructura hay dos radicales a la misma distancia del extremo pero el de menor orden alfabético es el fenil. Como es un radical todos los grupos funcionales como halógenos y también los enlaces múltiples son más importantes que él. Seleccionamos la cadena continua de carbonos más larga que tenga los carbonos unidos al bromo y al radical fenil. La numeración se inicia por el extremo donde está el bromo que es grupo funcional de haluros orgánicos.
Seleccionamos la cadena continua de carbonos más larga que tenga los carbonos unidos al bromo y al radical fenil. La numeración se inicia por el extremo donde está el bromo que es grupo funcional de haluros orgánicos. 1-BROMO-5-FENIL-4-ISOBUTILHEPTANO
1-BROMO-5-FENIL-4-ISOBUTILHEPTANO
.1 ÉteresLos éteres se consideran derivados del agua, donde los dos hidrógenos han sido sustituidos por radicales alquilo.Grupo funcional: –O–(OXA)Fórmula general: R–O–R’ donde R y R’ son radicales alquilo o arilo los cuales pueden ser iguales o diferentes.- La mayoría de los éteres son líquidos a temperatura ambiente. Solo es gas el metoximetano cuya estructura se muestra a continuación:

- En general su olor es agradable.
- Los éteres que tienen de cinco o menos átomos de carbono son soluble en agua. El resto son insolubles.
- Son menos densos que el agua (flotan sobre ella).
- Desde el punto de vista químico, son bastante inertes aunque en caliente reaccionan con ácido yodhídrico (HI).
Éter etílico.-Es el más importante de los éteres.También se le conoce como etoxietano, dietil éter o simplemente éter. Su fórmula es: Se utiliza como disolvente, en la fabricación de explosivos y en medicina como antiespasmódico.El éter etílico se empleaba anteriormente como anestésico, pero debido a que es muy inflamable y a los efectos secundarios, ha sido reemplazado por otras sustancias
Se utiliza como disolvente, en la fabricación de explosivos y en medicina como antiespasmódico.El éter etílico se empleaba anteriormente como anestésico, pero debido a que es muy inflamable y a los efectos secundarios, ha sido reemplazado por otras sustancias
Cuando el grupo oxa del éter está unido a dos radicales alquilo o arilo, sin ningún otro grupo funcional, se acostumbra nombrar los radicales y al final la palabra éter. Si los radicales son iguales el éter se dice que essimétrico o simple y si no es entonces asimétrico o mixto. Esta nomenclatura es de tipo común, pero por acuerdo ordenamos los radicales en orden alfabético.Ejemplos:Éteres simétricos:
DITER-BUTIL ÉTER DI-n-PROPIL ÉTER


DIETIL ÉTER DIISOPROPIL ÉTER 

Éteres asimétricos


ISOBUTIL METIL ÉTER n-BUTIL-n-PROPIL ÉTER 

SEC-BUTIL ETIL ÉTER FENILISOBUTIL ÉTER
De nombre a fórmula:
Sec-butil isobutil éter Isopropil-n-propil éter 

Se coloca el oxígeno como unión de los radicales. Verifique que sea en el enlace libre de cada radical donde se una el oxígeno. El lugar donde coloque los radicales es indistinto, lo importante es que esté el oxígeno entre ellos en la posición adecuada. Etil fenil éter n-butil metil éter 

Escriba la estructura o el nombre según corresponda para los siguientes compuestos: Revise sus resultados consultando la sección de respuestas.
a)b)c)d)e) disobutil éter
fenil-n-propil éter
n-butilisobutil éter
etilmetil éter
sec-butilter-butil éter
f) 
g) 
h) 
i) 
j) 
Resuelva en hojas blancas tamaño carta los siguientes ejercicios.I. Escriba la estructura que corresponda a los siguientes nombres.a) ISOBUTILISOPROPIL ÉTERb) TER-BUTIL-n-PROPILÉTERc) N-BUTILFENIL ÉTERd) ÉTER ETÍLICOII. Escriba el nombre que corresponda a las siguientes estructuras. Señale la cadena principal y su numeración.
a) 
b) 
c) 
d) 
e) 
Los alcoholes se pueden considerar compuestos derivados del agua, donde uno de sus hidrógeno ha sido reemplazado por un radical alquilo o arilo.
El grupo funcional es –OH cuyo nombre es HIDROXI.Esta clasificación se basa en el tipo de carbono al cual está unido el grupo –OH (hidroxi).PRIMARIOS.-Son aquellos alcoholes en los que el grupo –OH (hidroxi) está unido a un carbono primario, o sea un carbono unido a un solo carbono.Ejemplos:
 Los carbonos a los cuales está unido el grupo–OH (hidroxi) (rojos) están a su vez unidos a un solo carbono (azul), por tanto son primarios.SECUNDARIOS.- Son aquellos en los cuales el grupo –OH (hidroxi) está unido a un carbono secundario, o sea un carbono unido a dos átomos de carbono.Ejemplo:
Los carbonos a los cuales está unido el grupo–OH (hidroxi) (rojos) están a su vez unidos a un solo carbono (azul), por tanto son primarios.SECUNDARIOS.- Son aquellos en los cuales el grupo –OH (hidroxi) está unido a un carbono secundario, o sea un carbono unido a dos átomos de carbono.Ejemplo: El carbono unido al –OH (rojo) está enlazado a dos carbonos (azules), por tanto es un carbono secundario.TERCIARIOS.- Son aquellos en los cuales el grupo –OH (hidroxi) está unido a un carbono terciario, o sea un carbono unido a tres átomos de carbono.Ejemplo:
El carbono unido al –OH (rojo) está enlazado a dos carbonos (azules), por tanto es un carbono secundario.TERCIARIOS.- Son aquellos en los cuales el grupo –OH (hidroxi) está unido a un carbono terciario, o sea un carbono unido a tres átomos de carbono.Ejemplo: El carbono al cual está unido el grupo –OH (rojo) está unido a su vez a tres átomos de carbono (azules), el carbono es terciario.
El carbono al cual está unido el grupo –OH (rojo) está unido a su vez a tres átomos de carbono (azules), el carbono es terciario.
ALCOHOL METÍLICO O METANOL (CH3-OH)Propiedades:- Líquido incoloro de olor agradable si es puro.
- Muy soluble en agua.
- Altamente tóxico, provoca ceguera e incluso la muerte si se ingiere o aplica externamente.
Usos:- Se utiliza para desnaturalizar el alcohol etílico haciéndolo no potable.
- Como combustible y aditivo para gasolina, ya que su índice de octano es mayor al de la gasolina, además de que es más seguro y más limpio, por lo que contamina menos.
- Disolvente en la fabricación de barnices y pinturas.
ALCOHOL ETÍLICO O ETANOL (CH3-CH2-OH)Propiedades:- Líquido incoloro de olor característico.
- Sabor caústico y ardiente.
- Muy soluble en agua
- Arde con flama.
Usos:* Disolvente industrial de grasas, aceites y resinas.
* Desinfectante y antiséptico.
* En la fabricación de bebidas alcohólicasBebidas alcohólicasLas características de las bebidas alcohólicas dependen del origen de los azúcares fermentados así como del proceso de elaboración. Ejemplos:
BEBIDA ORIGEN Ron Caña de azúcar  html.rincondelvago.com/ cana-de-azucar.html
html.rincondelvago.com/ cana-de-azucar.htmlTequila Agave 
www.tropengarten.de/ Bilder/B-Agave-mk70.jpgMezcal Maguey 
www.homebrew.com/ wine_cellar/wineblog.shtmlWhisky Cebada 
www.floresdigitales.com/ g07/10.htmBrandy, cognac y vinos Uva  educar.sc.usp.br/ licenciatura/1999/uva.jpg
educar.sc.usp.br/ licenciatura/1999/uva.jpg
El etanol ingerido en exceso, provoca serios problemas: disminuye el autocontrol, la capacidad intelectual, los reflejos y otros trastornos propios del estado de ebriedad. Puede producir pérdida de la conciencia y finalmenteprovocar la muerte. Es muy importante analizar los graves efectos del estado ebrio. Un alto porcentaje de los accidentes automovilísticos, muchos de los cuales llegan a ser fatales o de graves consecuencias, son provocados por la ebriedad del conductor. Por esto es tan importante tener control en la forma de beber y hacerlo con responsabilidad y en caso de que haya un problema serio de alcoholismo, pedir ayuda con el fin de evitar un desenlace fatal. Las personas con problemas de alcoholismo pueden perder su familia, sus oportunidades de trabajo y llevar una vida muy lejos de la dignidad y respeto que merece la vidaun ser humano.PROPANOTRIOL O GLICERINA.-Es un polialcohol, o sea que tiene más de un grupo –OH en su estructura. Su fórmula es: Usos.-
Usos.-- Fabricación de nitroglicerina y resinas..
- Agente edulcorante y humectante en confitería.
- En la elaboración de cosméticos, cremas y algunos jabones.
- Lubricante en productos farmacéuticos.
ETILENGLICOL O GLICEROL.-Es un diol, o sea que contiene dos grupos –OH en su estructura. Su fórmula es: Es muy utilizado como anticongelante y en la elaboración de una fibra sintética conocida como dacrón.FENOL O HIDROXIBENCENO.-Es el alcohol aromático más sencillo.
Es muy utilizado como anticongelante y en la elaboración de una fibra sintética conocida como dacrón.FENOL O HIDROXIBENCENO.-Es el alcohol aromático más sencillo. Usos.-Fabricación de plásticosPreparación de antisépticos usados en pastillas para la garganta y enjuagues bucales.Elaboración de desinfectantes para el hogar.Lectura:
Usos.-Fabricación de plásticosPreparación de antisépticos usados en pastillas para la garganta y enjuagues bucales.Elaboración de desinfectantes para el hogar.Lectura:
Lea el texto tiludado: "Alcohol etílico". Elabore un comentario de la lectura y mándelo al correo elelctrónico dle profesor.
Nomenclatura común de alcoholes.-Cuando el alcohol se deriva de un grupo alquilo se utilizan un nombre común formado por la palabra ALCOHOL y el nombre del radical añadiéndole la terminación ICO.Ejemplos:

ALCOHOL METÍLICO 
ALCOHOL ETÍLICO 
ALCOHOL n-PROPÍLICO 
ALCOHOL ISOPROPÍLICO 
ALCOHOL n-BUTÍLICO 
ALCOHOL ISOBUTÍLICO 
ALCOHOL SEC-BUTÍLIVO 
ALCOHOL TER-BUTÍLICO
Nomenclatura sistémica de alcoholes.-La terminación sistémica de los alcoholes es OL. El alcohol es el más importante de los grupos funcionales que hemos estudiado y la numeración de la cadena debe iniciarse por el extremo más cercano al carbono que tiene el radical -OH (hidroxi) pero en la cadena deben incluirse todos los carbonos unidos a algún grupo funcional o al radical fenil.Ejemplos de fórmula a nombre:
a) 

Se selecciona la cadena más larga que contenga el carbono unido al grupo –OH e iniciamos su numeración por el extremo más cercano a ese carbono. Se nombran los radicales en orden alfabético, y al final el nombre de la cadena principal con terminación ol indicando la posición de el grupo hidroxi.4-METIL-2-HEXANOL. b) 

En este caso, la cadena de carbonos continúa más larga que contiene todos los carbonos unidos a un grupo funcional es horizontal. Como el grupo –OH está exactamente a la mitad de la cadena, tomamos como referencia el siguiente grupo funcional que es el átomo de bromo.1-BROMO-3-ISOBUTIL-4-HEPTANOL
c) 

2-FENIL-5-METIL-4-OCTANOL
d) 

3-ETIL-4-METIL-1-PENTANOL
e) 

En este caso, la cadena más larga es la horizontal, ya que si el radical sec-butil se incluyera en la cadena quedaria fuera el carbono que tiene cloro.
3-SEC-BUTIL-4-CLORO-1-BUTANOL
De nombre a estructura:a) 4,4,-dimetil-2-hexanolEs una cadena de 6 carbonos. Tiene dos metiles en el carbono 3. La terminación ol indica que hay un grupo –OH unido a uno de los carbonos de la cadena, que en este caso es el carbono#2, ya que este número antecede a la palabra hexanol. b) 1,6-dibromo-5-ter-butil-3-heptanolEs una cadena de 7 carbonos con un grupo –OH característico del alcohol en la posición 3.
b) 1,6-dibromo-5-ter-butil-3-heptanolEs una cadena de 7 carbonos con un grupo –OH característico del alcohol en la posición 3. c) 1,2,2,8-tetracloro-4-etil-4-nonanolCadena de 9 carbonos con un grupo OH en el carbono # 4.
c) 1,2,2,8-tetracloro-4-etil-4-nonanolCadena de 9 carbonos con un grupo OH en el carbono # 4.
d) 2-ter-butil-5,6,-dimetil-6-yodo-4-octanol e) 2,8,10-tribromo-3-sec-butil-5-decanol
e) 2,8,10-tribromo-3-sec-butil-5-decanol
Escriba la estructura o el nombre según corresponda para los siguientes compuestos. Comprueba sus resultados en la sección de respuestas al final del capítulo.a) 4-cloro-3-isopropil-1-pentanolb) 2-metil-4-etil-4-heptanolc) 4-isobutil-4-n-propil-3-octanold) Alcohol terbutílicoe) 4-bromo-2-sec-butil-1-butanol
f) 
g) 
h) 
i) 
j) 
TAREA 3.7
Resuelva los siguientes ejercicios en hojas blancas tamaño carta y entréguelo a su profesor en la fecha por el señalada.I. ESCRIBA LA ESTRUCTURA QUE CORRESPONDA A LOS SIGUIENTES NOMBRES.1) 2,4,5-TRIMETIL-3-HEXANOL2) 4-TER-BUTIL-5-ISOPROPIL-2-OCTANOL3) 1-BROMO-5-CLORO-6-ETIL-3-PENTANOL4) 3-ISOBUTIL-5-METIL-1-HEPTANOL5) 3-FENIL-1-BUTANOLII. ESCRIBA EL NOMBRE QUE CORRESPONDA A LAS SIGUIENTES ESTRUCTURAS. SEÑALE LA CADENA PRINCIPAL Y SU NUMERACIÓN.
a) 
b) 
c) 
d) 
e) 
EJERCICIO 3.8Ejercicio de integraciónI. ESCRIBA LA ESTRUCTURA CORRECTA PARA CADA UNO DE LOS SIGUIENTE NOMBRES. ESCRIBA ENTRE PARÉNTESIS EL NÚMERO QUE CORRESPONDA AL TIPO DE COMPUESTO DE ACUERDO A LA SIGUIENTE CLAVE:
01) Alcano 04) Alquino 02) Haluro orgánico 05) Éter 03) Alqueno 06) Alcohol
1) SEC-BUTILMETIL ÉTER2) 6-BROMO-4-ISOBUTIL-2-METIL-3-HEPTENO3) 2-BROMO-3-TER-BUTIL-7-ETILNONANO4) DIISOBUTIL ÉTER5) 3-n-BUTIL-4-ISOPROPIL-1-OCTINO6) 6-ETIL-4-ISOPROPIL-2-METILNONANO7) YODURO DE SEC-BUTILO8) ACETILENO9) ISOBUTIL ISOPROPIL ÉTER10) ALCOHOL METÍLICOII. ESCRIBA EL NOMBRE DE CADA ESTRUCTURA Y ANOTE ENTRE PARÉNTESIS EL NUMERO CORRESPONDIENTE AL TIPO DE COMPUESTO CON LA CLAVE UTILIZADA EN EL EJERCICIO ANTERIOR.
a) b) 

c) d) 

e) f) 

g) h) 

i) j) 

I. En una hoja blanca tamaño carta, dibuje la estructura correcta para los siguientes compuestos, indicando sobre la línea el tipo de compuestos: alcano, alqueno, alquino, haluro orgánica, aromático, éster o alcohol.1) 3-ter-butil-6-metil1-heptino_______________2) 6-cloro-3-isopropil-2-hexanol_______________3) m-aminohidroxibenceno_______________4) n-butilter-butil éter_______________5) 2-bromo-3-clorobutano_________________II. En una hoja blanca tamaño carta, complete la siguiente tabla con la información solicitada escribiendo debajo de cada estructura su nombre correcto.Indique la cadena principal y su numeración.
Estructura Tipo de compuesto a) 
b) 
c) 
d) 
e) 
Disustituidos
Benceno como radical
Aromáticos Policíclicos



Se emplea en la fabricación de explosivos y colorantes.

Este compuesto no tiene nombre común. Es un líquido incoloro de olor agradable empleado en la fabricación del fenol y del DDT.

Fue el primer desinfectante utilizado, pero por su toxicidad ha sido reemplazado por otros menos perjudiciales.
Se emplea para preparar medicamentos, perfumes, fibras textiles artificiales, en la fabricación de colorantes. En aerosol, se utiliza para tratar irritaciones de la garganta. En concentraciones altas es venenoso.

Es la amina aromática más importante. Es materia prima para la elaboración de colorantes que se utilizan en la industria textil. Es un compuesto tóxico.

Se emplea como materia prima de sustancias tales como colorantes. Se utiliza en la fabricación de trinitrotolueno (TNT) un explosivo muy potente.

Se utiliza como desinfectante y como conservador de alimentos.

Es conocido vulgarmente como nafltalina. Es utilizado en germicidas y parasiticidas, además de combatir la polilla.

Se utiliza para proteger postes y durmientes de ferrocarril de agentes climatológicos y del ataque de insectos.

Agente cancerígeno presente en el humo del tabaco.




Los sustituyentes están en dos carbonos seguidos.
Hay un carbono sin sustituyente, entre los que tienen un sustituyente.
Los sustituyentes están en posiciones encontradas,.
Posiciones
Posiciones
Posiciones
1,2
2,3
3,4
4,5
5,6
6,1
1,3
2,5
3,5
5,1
1,4
2,5
3,6

La posición es meta porque hay un carbono sin sustituyente entre ellos. Esta posición se indica con la letra “m” minúscula y los sustituyentes se acomodan en orden alfabético uniendo la final la palabra benceno y se escribe como una sola palabra Observe que se pone un guión entre la letra de la posición y el nombre del compuesto.
m-CLOROMETILBENCENO

Los sustituyentes están encontrados, por lo tanto la posición es para. Se pone la “p” minúscula, y acomodando los radicales en orden alfabético y al final la palabra benceno.
p-HIDROXIISOPROPILBENCENO

Los sustituyentes se encuentran en carbonos contiguos, por lo tanto la posición es orto “o”. Se acomodan los sustituyentes en orden alfabético y al final la palabra benceno.
o-AMINOISOBUTILBENCENO
m-etilnitrobenceno
Primero ponemos el anillo y elegimos cualquiera de la posiciones meta y los sustituyentes se pueden colocar indistintamente.

p-aminoyodobenceno
Ponemos el anillo con sustituyentes en posición para, encontrados y colocamos el yodo y el grupo amino indistintamente.

o-sec-butilhidroxibenceno
Se colocan dos sustituyentes en carbonos contiguos en un anillo aromático y se colocan el yodo y el grupo hidroxi en forma indistinta.

a)

b)

c)

d)

e)

f)

g)
m-cloroyodobenceno
h)
o-isobutilisopropilbenceno
i)
phidroxinitrobenceno
j)
m-aminosec-butilbenceno
- El número 1 corresponde al radical con menor orden alfabético.
- La numeración debe continuarse hacia donde este el radical más cercano para obtener la serie de números más pequeña posible. Si hay dos radicales a la misma distancia, se selecciona el de menor orden alfabético; si son iguales se toma el siguiente radical más cercano.
- Todos los átomos de carbono deben numerarse, no solo los que tengan sustituyente.
- Al escribir el nombre se ponen los radicales en orden alfabético terminando con la palabra benceno.
- Como en los compuestos alifáticos, utilizamos comas para separar números y guiones para separar números y palabras.

El número 1 corresponde al bromo que es el radical de menor orden alfabético. Se numera hacia la derecha porque en ese sentido quedan los números más pequeños posibles .
1-bromo-3-etil-4-metilbenceno

El radical de menor orden alfabético es el hidroxi, pero a la misma distancia haya dos radicales, por tanto elegimos el nitro que es el de menor orden alfabético y continuamos la numeración en ese sentido.
1-hidroxi-2-nitro-6-n-propilbenceno

El radical de menor orden alfabético es el sec-butil (recuerde que se alfabetiza por la “b”). Iniciamos ahí la numeración y la continuamos hacia el cloro que es el radical más cercano.
1-sec-butil-2-cloro-4-nitrobenceno

El número 1 coresponde al radical de menor orden alfabético, que es el n-butil. La numeración se continúa hacia la derecha porque el sec-butil tiene menor orden que el ter-butil y ambos están a la misma distancia del número 1.

El número 1 corresponde al amino que es el de menor orden alfabético. A la misma distancia hay un radical isopropil y un radical nitro. Numeramos hacia el isopropil porque tiene menor orden alfabético que el radical nitro. Nombramos en orden alfabético separando las palabras de los números con un guión.
1-amino-4-hidroxi-3-isopropil-
5-nitrobenceno
5-nitrobenceno
1,4-dimetil-2-n-propilbenceno

Dibujamos el anillo y lo numeramos. El número 1 se puede colocar en cualquier posición, y por acuerdo numeramos en el sentido de las manecillas del reloj. Podría numerarse en sentido contrario, por eso establecemos que es por acuerdo, no es una regla. Colocamos los radicales en las posiciones indicadas por los números.

No olvide que el anillo hexagonal del benceno tiene 3 dobles enlaces alternados. Iniciamos la numeración en el carbono de nuestra elección, hacia la derecha y colocamos los radicales.
1-etil-3-isopropil-4-yodobenceno


1-amino-2-bromo-6-isobutil-3-nitrobenceno


a)

b)

c)

d)

e)

f)

g)
h)
i)
j)
k)
a)

b)

c)

d)

e)

f)





.1 Éteres
Los éteres se consideran derivados del agua, donde los dos hidrógenos han sido sustituidos por radicales alquilo.
Grupo funcional: –O–(OXA)
Fórmula general: R–O–R’ donde R y R’ son radicales alquilo o arilo los cuales pueden ser iguales o diferentes.
- La mayoría de los éteres son líquidos a temperatura ambiente. Solo es gas el metoximetano cuya estructura se muestra a continuación:
- En general su olor es agradable.
- Los éteres que tienen de cinco o menos átomos de carbono son soluble en agua. El resto son insolubles.
- Son menos densos que el agua (flotan sobre ella).
- Desde el punto de vista químico, son bastante inertes aunque en caliente reaccionan con ácido yodhídrico (HI).
Éter etílico.-
Es el más importante de los éteres.También se le conoce como etoxietano, dietil éter o simplemente éter. Su fórmula es:
Se utiliza como disolvente, en la fabricación de explosivos y en medicina como antiespasmódico.
El éter etílico se empleaba anteriormente como anestésico, pero debido a que es muy inflamable y a los efectos secundarios, ha sido reemplazado por otras sustancias
Cuando el grupo oxa del éter está unido a dos radicales alquilo o arilo, sin ningún otro grupo funcional, se acostumbra nombrar los radicales y al final la palabra éter. Si los radicales son iguales el éter se dice que essimétrico o simple y si no es entonces asimétrico o mixto. Esta nomenclatura es de tipo común, pero por acuerdo ordenamos los radicales en orden alfabético.
Ejemplos:
Éteres simétricos:
DITER-BUTIL ÉTER | DI-n-PROPIL ÉTER |
 | |
DIETIL ÉTER | DIISOPROPIL ÉTER |
 |  |
Éteres asimétricos
 |  |
ISOBUTIL METIL ÉTER | n-BUTIL-n-PROPIL ÉTER |
 |  |
SEC-BUTIL ETIL ÉTER | FENILISOBUTIL ÉTER |
De nombre a fórmula:
Sec-butil isobutil éter | Isopropil-n-propil éter |
 |  |
Se coloca el oxígeno como unión de los radicales. Verifique que sea en el enlace libre de cada radical donde se una el oxígeno. | El lugar donde coloque los radicales es indistinto, lo importante es que esté el oxígeno entre ellos en la posición adecuada. |
Etil fenil éter | n-butil metil éter |
 |
Escriba la estructura o el nombre según corresponda para los siguientes compuestos: Revise sus resultados consultando la sección de respuestas.
a) b) c) d) e) | disobutil éter fenil-n-propil éter n-butilisobutil éter etilmetil éter sec-butilter-butil éter |
f) |  | g) |  |
h) |  | i) |  |
j) |  | ||
Resuelva en hojas blancas tamaño carta los siguientes ejercicios.
I. Escriba la estructura que corresponda a los siguientes nombres.
a) ISOBUTILISOPROPIL ÉTER
b) TER-BUTIL-n-PROPILÉTER
c) N-BUTILFENIL ÉTER
d) ÉTER ETÍLICO
II. Escriba el nombre que corresponda a las siguientes estructuras. Señale la cadena principal y su numeración.
a) |  | b) |  |
c) |  | d) |  |
e) |  |
Los alcoholes se pueden considerar compuestos derivados del agua, donde uno de sus hidrógeno ha sido reemplazado por un radical alquilo o arilo.
El grupo funcional es –OH cuyo nombre es HIDROXI.
Esta clasificación se basa en el tipo de carbono al cual está unido el grupo –OH (hidroxi).
PRIMARIOS.-Son aquellos alcoholes en los que el grupo –OH (hidroxi) está unido a un carbono primario, o sea un carbono unido a un solo carbono.
Ejemplos:

Los carbonos a los cuales está unido el grupo–OH (hidroxi) (rojos) están a su vez unidos a un solo carbono (azul), por tanto son primarios.
SECUNDARIOS.- Son aquellos en los cuales el grupo –OH (hidroxi) está unido a un carbono secundario, o sea un carbono unido a dos átomos de carbono.
Ejemplo:

El carbono unido al –OH (rojo) está enlazado a dos carbonos (azules), por tanto es un carbono secundario.
TERCIARIOS.- Son aquellos en los cuales el grupo –OH (hidroxi) está unido a un carbono terciario, o sea un carbono unido a tres átomos de carbono.
Ejemplo:

El carbono al cual está unido el grupo –OH (rojo) está unido a su vez a tres átomos de carbono (azules), el carbono es terciario.
ALCOHOL METÍLICO O METANOL (CH3-OH)
Propiedades:
- Líquido incoloro de olor agradable si es puro.
- Muy soluble en agua.
- Altamente tóxico, provoca ceguera e incluso la muerte si se ingiere o aplica externamente.
Usos:
- Se utiliza para desnaturalizar el alcohol etílico haciéndolo no potable.
- Como combustible y aditivo para gasolina, ya que su índice de octano es mayor al de la gasolina, además de que es más seguro y más limpio, por lo que contamina menos.
- Disolvente en la fabricación de barnices y pinturas.
ALCOHOL ETÍLICO O ETANOL (CH3-CH2-OH)
Propiedades:
- Líquido incoloro de olor característico.
- Sabor caústico y ardiente.
- Muy soluble en agua
- Arde con flama.
Usos:
* Disolvente industrial de grasas, aceites y resinas.
* Desinfectante y antiséptico.
* En la fabricación de bebidas alcohólicas
* Desinfectante y antiséptico.
* En la fabricación de bebidas alcohólicas
Bebidas alcohólicas
Las características de las bebidas alcohólicas dependen del origen de los azúcares fermentados así como del proceso de elaboración. Ejemplos:
BEBIDA | ORIGEN | |
Ron | Caña de azúcar |  html.rincondelvago.com/ cana-de-azucar.html |
Tequila | Agave |  www.tropengarten.de/ Bilder/B-Agave-mk70.jpg |
Mezcal | Maguey |  www.homebrew.com/ wine_cellar/wineblog.shtml |
Whisky | Cebada |  www.floresdigitales.com/ g07/10.htm |
Brandy, cognac y vinos | Uva |  educar.sc.usp.br/ licenciatura/1999/uva.jpg |
El etanol ingerido en exceso, provoca serios problemas: disminuye el autocontrol, la capacidad intelectual, los reflejos y otros trastornos propios del estado de ebriedad. Puede producir pérdida de la conciencia y finalmenteprovocar la muerte. Es muy importante analizar los graves efectos del estado ebrio. Un alto porcentaje de los accidentes automovilísticos, muchos de los cuales llegan a ser fatales o de graves consecuencias, son provocados por la ebriedad del conductor. Por esto es tan importante tener control en la forma de beber y hacerlo con responsabilidad y en caso de que haya un problema serio de alcoholismo, pedir ayuda con el fin de evitar un desenlace fatal. Las personas con problemas de alcoholismo pueden perder su familia, sus oportunidades de trabajo y llevar una vida muy lejos de la dignidad y respeto que merece la vidaun ser humano.
PROPANOTRIOL O GLICERINA.-
Es un polialcohol, o sea que tiene más de un grupo –OH en su estructura. Su fórmula es:

Usos.-
- Fabricación de nitroglicerina y resinas..
- Agente edulcorante y humectante en confitería.
- En la elaboración de cosméticos, cremas y algunos jabones.
- Lubricante en productos farmacéuticos.
ETILENGLICOL O GLICEROL.-
Es un diol, o sea que contiene dos grupos –OH en su estructura. Su fórmula es:

Es muy utilizado como anticongelante y en la elaboración de una fibra sintética conocida como dacrón.
FENOL O HIDROXIBENCENO.-
Es el alcohol aromático más sencillo.

Usos.-
Fabricación de plásticos
Preparación de antisépticos usados en pastillas para la garganta y enjuagues bucales.
Elaboración de desinfectantes para el hogar.
Lectura:
Lea el texto tiludado: "Alcohol etílico". Elabore un comentario de la lectura y mándelo al correo elelctrónico dle profesor.
Lea el texto tiludado: "Alcohol etílico". Elabore un comentario de la lectura y mándelo al correo elelctrónico dle profesor.
Nomenclatura común de alcoholes.-
Cuando el alcohol se deriva de un grupo alquilo se utilizan un nombre común formado por la palabra ALCOHOL y el nombre del radical añadiéndole la terminación ICO.
Ejemplos:
ALCOHOL METÍLICO | |
ALCOHOL ETÍLICO | |
ALCOHOL n-PROPÍLICO | |
 | ALCOHOL ISOPROPÍLICO |
ALCOHOL n-BUTÍLICO | |
 | ALCOHOL ISOBUTÍLICO |
 | ALCOHOL SEC-BUTÍLIVO |
 | ALCOHOL TER-BUTÍLICO |
Nomenclatura sistémica de alcoholes.-
La terminación sistémica de los alcoholes es OL. El alcohol es el más importante de los grupos funcionales que hemos estudiado y la numeración de la cadena debe iniciarse por el extremo más cercano al carbono que tiene el radical -OH (hidroxi) pero en la cadena deben incluirse todos los carbonos unidos a algún grupo funcional o al radical fenil.
Ejemplos de fórmula a nombre:
| a) |  |  |
Se selecciona la cadena más larga que contenga el carbono unido al grupo –OH e iniciamos su numeración por el extremo más cercano a ese carbono. Se nombran los radicales en orden alfabético, y al final el nombre de la cadena principal con terminación ol indicando la posición de el grupo hidroxi. 4-METIL-2-HEXANOL . | ||
| b) |  |  |
En este caso, la cadena de carbonos continúa más larga que contiene todos los carbonos unidos a un grupo funcional es horizontal. Como el grupo –OH está exactamente a la mitad de la cadena, tomamos como referencia el siguiente grupo funcional que es el átomo de bromo. 1-BROMO-3-ISOBUTIL-4-HEPTANOL | ||
| c) |  |  |
2-FENIL-5-METIL-4-OCTANOL | ||
| d) |  |  |
3-ETIL-4-METIL-1-PENTANOL | ||
| e) |  |  |
| En este caso, la cadena más larga es la horizontal, ya que si el radical sec-butil se incluyera en la cadena quedaria fuera el carbono que tiene cloro. 3-SEC-BUTIL-4-CLORO-1-BUTANOL | ||
De nombre a estructura:
a) 4,4,-dimetil-2-hexanol
Es una cadena de 6 carbonos. Tiene dos metiles en el carbono 3. La terminación ol indica que hay un grupo –OH unido a uno de los carbonos de la cadena, que en este caso es el carbono#2, ya que este número antecede a la palabra hexanol.

b) 1,6-dibromo-5-ter-butil-3-heptanol
Es una cadena de 7 carbonos con un grupo –OH característico del alcohol en la posición 3.

c) 1,2,2,8-tetracloro-4-etil-4-nonanol
Cadena de 9 carbonos con un grupo OH en el carbono # 4.

d) 2-ter-butil-5,6,-dimetil-6-yodo-4-octanol

e) 2,8,10-tribromo-3-sec-butil-5-decanol

Escriba la estructura o el nombre según corresponda para los siguientes compuestos. Comprueba sus resultados en la sección de respuestas al final del capítulo.
a) 4-cloro-3-isopropil-1-pentanol
b) 2-metil-4-etil-4-heptanol
c) 4-isobutil-4-n-propil-3-octanol
d) Alcohol terbutílico
e) 4-bromo-2-sec-butil-1-butanol
f) |  | g) |  |
h) |  | i) |  |
j) |  | ||
TAREA 3.7
Resuelva los siguientes ejercicios en hojas blancas tamaño carta y entréguelo a su profesor en la fecha por el señalada.
I. ESCRIBA LA ESTRUCTURA QUE CORRESPONDA A LOS SIGUIENTES NOMBRES.
1) 2,4,5-TRIMETIL-3-HEXANOL
2) 4-TER-BUTIL-5-ISOPROPIL-2-OCTANOL
3) 1-BROMO-5-CLORO-6-ETIL-3-PENTANOL
4) 3-ISOBUTIL-5-METIL-1-HEPTANOL
5) 3-FENIL-1-BUTANOL
II. ESCRIBA EL NOMBRE QUE CORRESPONDA A LAS SIGUIENTES ESTRUCTURAS. SEÑALE LA CADENA PRINCIPAL Y SU NUMERACIÓN.
a) |  | b) |  |
c) |  | d) |  |
e) |  |
EJERCICIO 3.8
Ejercicio de integración
I. ESCRIBA LA ESTRUCTURA CORRECTA PARA CADA UNO DE LOS SIGUIENTE NOMBRES. ESCRIBA ENTRE PARÉNTESIS EL NÚMERO QUE CORRESPONDA AL TIPO DE COMPUESTO DE ACUERDO A LA SIGUIENTE CLAVE:
01) | Alcano | 04) | Alquino |
02) | Haluro orgánico | 05) | Éter |
03) | Alqueno | 06) | Alcohol |
1) SEC-BUTILMETIL ÉTER
2) 6-BROMO-4-ISOBUTIL-2-METIL-3-HEPTENO
3) 2-BROMO-3-TER-BUTIL-7-ETILNONANO
4) DIISOBUTIL ÉTER
5) 3-n-BUTIL-4-ISOPROPIL-1-OCTINO
6) 6-ETIL-4-ISOPROPIL-2-METILNONANO
7) YODURO DE SEC-BUTILO
8) ACETILENO
9) ISOBUTIL ISOPROPIL ÉTER
10) ALCOHOL METÍLICO
II. ESCRIBA EL NOMBRE DE CADA ESTRUCTURA Y ANOTE ENTRE PARÉNTESIS EL NUMERO CORRESPONDIENTE AL TIPO DE COMPUESTO CON LA CLAVE UTILIZADA EN EL EJERCICIO ANTERIOR.
a) | b) |
 |  |
c) | d) |
 |  |
e) | f) |
 | |
g) | h) |
 |  |
i) | j) |
 |
I. En una hoja blanca tamaño carta, dibuje la estructura correcta para los siguientes compuestos, indicando sobre la línea el tipo de compuestos: alcano, alqueno, alquino, haluro orgánica, aromático, éster o alcohol.
1) 3-ter-butil-6-metil1-heptino_______________
2) 6-cloro-3-isopropil-2-hexanol_______________
3) m-aminohidroxibenceno_______________
4) n-butilter-butil éter_______________
5) 2-bromo-3-clorobutano_________________
II. En una hoja blanca tamaño carta, complete la siguiente tabla con la información solicitada escribiendo debajo de cada estructura su nombre correcto.Indique la cadena principal y su numeración.
Estructura | Tipo de compuesto | |
a) |  | |
b) |  | |
c) |  | |
d) |  | |
| e) |  | |